Главные внутренние факторы протекания электрохимической коррозии
На интенсивность распространения коррозийного поражения влияют две группы факторов – внешние и внутренние.
Текущее состояние поверхности металла
Когда поверхность металла неровная, коррозийный процесс протекает намного интенсивнее. Если на поверхности присутствуют небольшие выступы, они начинают накапливать воду.
Это может негативно повлиять на интенсивность распространения.
Чтобы не допустить такого фактора, важно использовать отшлифованный или отполированный металл. Когда сталь гладкая, вода не так сильно повреждает ее, потому что постепенно происходит формирование равномерной пленки по всей поверхности
Когда сталь гладкая, вода не так сильно повреждает ее, потому что постепенно происходит формирование равномерной пленки по всей поверхности.
Также хорошим средством для уменьшения поражения становится применение пассивирования, а также ряд других способов.
Степень термодинамической стойкости металла
Разные виды материалов отличаются разными показателями термодинамической устойчивости.
Наиболее стойкие разновидности материала не разрушаются при помещении в агрессивную среду.
Именно такой фактор оказывает большое влияние на потенциальное воздействие среды на постепенное развитие коррозии.
К сожалению, у большинства представленных в продаже марок металлов стойкость невысокая. Есть и неустойчивые разновидности, у которых этот риск нивелируется благодаря склонности к образованию пассивных пленок на поверхности.
Кристаллографическая структура
Оказывает прямое воздействие на металл.
Как известно, атомы в кристаллической решетке располагаются по-разному. Лучше защищены те разновидности, у которых атомы упакованы неплотно.
Особенности решетки также учитывают при планировании защиты материала методом создания на нем специальных пленок. И пленка и сам основной материал должны четко соответствовать по составу друг другу или быть максимально приближенными.
В этом случае исключается появление напряжения, которое негативно отражается на текущем состоянии заготовки. Если контакт с агрессивной средой все-таки происходит, материал начинает разрушаться слой за слоем.
Гетерогенность
Этот фактор рассматривается в непосредственной связи с величиной зерна металла.
Если в сплаве есть выраженные анодные включения, они сильно влияют на ускорение протекания коррозии.
Катодные включения не столь опасны, потому что на интенсивности процесса не отражаются. Величина зерна как фактор риска рассматривается не так часто и этим показателем можно пренебречь.
Коррозия меди в воде
Скорость коррозии меди в воде во многом зависит от наличия на поверхности оксидных пленок.
В быстро движущихся водных растворах и воде медь подвергается такому виду разрушения, как ударная коррозия. Скорость протекания ударной коррозии меди сильно зависит от количества растворенного кислорода. Если вода сильно аэрирована – ударная коррозия меди протекает интенсивно, если же обескислорожена – разрушение незначительно. Коррозия меди в аэрированной воде усиливается с уменьшением рН, увеличением концентрации ионов хлора. Скорость коррозии меди в воде зависит от климатической зоны. В тропиках скорость разрушения несколько выше.
Особенностью меди, омываемой морской водой, можно считать то, что она является одним из немногих металлов, которые не подвержены обрастанию микроорганизмами. Ионы меди для них губительны.
С чистой меди очень часто изготавливают трубопроводы для подачи в дома воды. Они надежны, служат очень долгое время. При наличии в воде растворенной угольной и других кислот медь понемногу корродирует, а продукты коррозии меди окрашивают сантехническое оборудование. Если вода, проходящая через медные трубы контактирует с железом, алюминием или оцинкованной сталью – то коррозию этих металлов значительно усиливается. Ионы меди осаждаются на поверхности этих металлов, образуя коррозионные гальванические элементы.
Чтоб исключить вредное влияние воды с медных труб на другие металлы используют луженую медь. Внутреннюю часть медного трубопровода покрывают оловом. Оловянное покрытие должно быть безпористым, во избежание возникновения гальванического элемента (олово по отношению к меди является катодом).
Современные методы борьбы
Многочисленные исследования и развитие технического прогресса привели к созданию целой системы методов и средств в борьбе с коррозией. Можно отметить три основных направления в защите от коррозии:
- Конструктивные решения.
- Активные методы.
- Пассивные методы.
Конструктивные решения состоят в выборе материалов, которые минимально поддаются коррозии по своим физическим свойствам:
- нержавеющие стали;
- легированные стали;
- цветные металлы.
 Активные методы борьбы подсказала сама электрохимическая коррозия. Постоянное напряжение прикладывают к защищаемой металлической конструкции так, чтобы повысить его электродный потенциал и замедлить процесс электрохимического растворения. Второй вариант активной защиты — жертвенный анод, который имеет низкий электродный потенциал, вследствие чего разрушается вместо защищаемого объекта.
Активные методы борьбы подсказала сама электрохимическая коррозия. Постоянное напряжение прикладывают к защищаемой металлической конструкции так, чтобы повысить его электродный потенциал и замедлить процесс электрохимического растворения. Второй вариант активной защиты — жертвенный анод, который имеет низкий электродный потенциал, вследствие чего разрушается вместо защищаемого объекта.
Пассивные методы состоят в нанесении защитных покрытий. Технический прогресс в этой области начал развиваться с нанесения простейших лакокрасочных покрытий, предотвращающих попадания кислорода, влаги и конденсата на поверхность металлов. Затем появились гальванические покрытия на основе:
- цинка — цинкование;
- хрома — хромирование;
- никеля — никелирование.
Оцинкованное железо, никелированные и хромированные столовые приборы, консервные банки с продуктами служат многие годы, не поддаваясь электрохимической коррозии, сохраняя красивый внешний вид, предохраняя порчу продуктов.
Методы защиты металлов от коррозии
Для защиты металлов от коррозии применяются различные методы: легирование металлов, обработка коррозионной среды, электрохимическая защита, нанесение металлических и неметаллических покрытий.
Легирование металлов позволяет получать коррозионностойкие сплавы, превосходящие по стойкости основной металл. Примерами могут служить сплавы меди (латунь и бронза), ее легирование алюминием для повышения коррозионной стойкости в атмосферных условиях; легирование стали хромом и никелем с целью создания хромоникелевых сплавов.
Обработку коррозионной среды выполняют с целью уменьшения ее агрессивного воздействия на металл. Однако такая обработка целесообразна при небольших объемах электролитов. Обработка среды заключается во введении в среду ингибиторов коррозии или в уменьшении содержания деполяризатора в электролитах.
Ингибиторы коррозии, введенные в коррозионную среду в малых количествах, полностью предотвращают коррозию металлов или значительно снижают ее скорость. В зависимости от характера среды ингибиторы выступают как замедлители кислотной или щелочной коррозии, коррозии в нейтральных растворах, в неводных средах. В основном, ингибиторы являются органическими соединениями.
Электрохимическая защита подразделяется на катодную и анодную защиту. Катодная защита подразделяется на защиту внешним током и протекторную защиту.
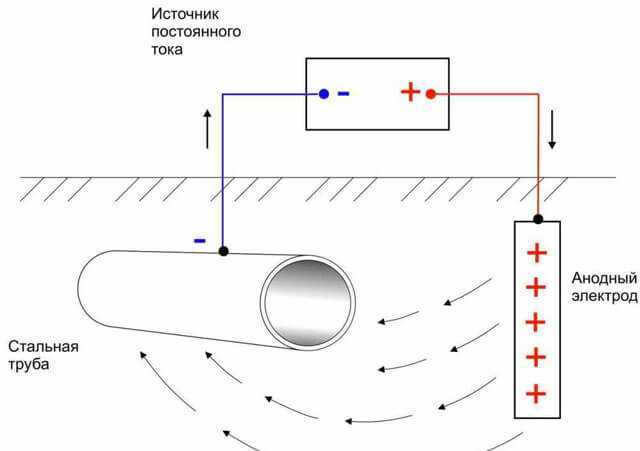
Механизм защиты внешним током (рис. 1) сводится к тому, что за счет внешней катодной поляризации защищаемому металлу навязывают потенциал, при котором его коррозия замедляется. Суть этого способа заключается в том, что защищаемую конструкцию подсоединяют к отрицательному полюсу внешнего источника постоянного тока, а к положительному полюсу подсоединяют электрод, которым может являться металлолом, а именно отрезок стальной трубы, рельсы и т. п. (рис. 1).
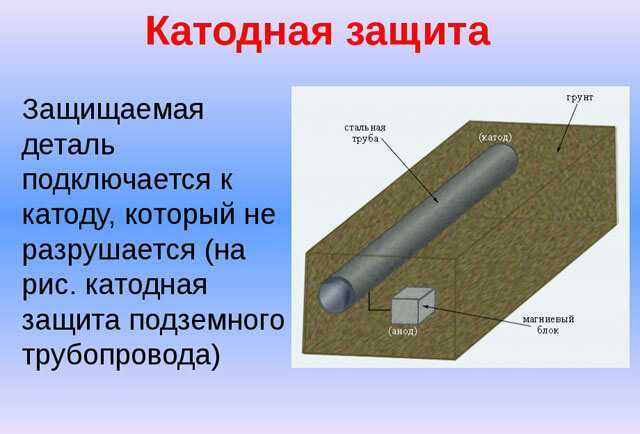
Протекторная защита (рис. 2) состоит в том, что к защищаемой конструкции подсоединяют металл или сплав, электродный потенциал которого более электроотрицателен, чем потенциал металла защищаемой конструкции. В качестве протекторов обычно используют цинк или сплавы цинка с алюминием. Иногда применяют сплавы на основе магния. Протекторы применяют для защиты металлических конструкций от коррозии в морской воде, других нейтральных коррозионных средах, а также в почве.
Рис. 1. Схема катодной защиты внешним током: 1 – источник постоянного тока; 2 – соединительный провод; 3 – пункт дренажа; 4 – защищаемая труба; 5 – изолирующее покрытие; 6 – анодное заземление; 7 – соединительный провод
Рис. 2. Схема протекторной защиты: 1 – подземная стальная конструкция; 2 – протектор–магниевый сплав; 3 – заполнитель; 4 – электрический контакт; 5 – контрольно-измерительный вывод; 6 – закороченные клеммы; Iп.з – сила тока протекторной защиты
Защита металлическими и неметаллическими покрытиями. Для защиты металлов от коррозии используют различные виды покрытий: металлические, лакокрасочные и полимерные покрытия и покрытия, образованные в результате химической или электрохимической обработки поверхности металла. Роль любого покрытия сводится в основном к изоляции металла от внешней среды.
Выбор типа покрытия зависит от условий, в которых следует использовать металл. Для защиты изделий, не подвергающихся механическим воздействиям и применяющимся в сухих жилых помещениях, обычно бывает достаточно однослойного лакокрасочного покрытия или соответствующей химической обработки поверхности металла: оксидирования или фосфатирования. Для защиты металлических конструкций (железнодорожные мосты, подъемные краны и т. п.), а также железнодорожных вагонов, наружных деталей автомобилей, велосипедов и др., подвергающихся воздействию влажной атмосферы, применяют сложные по составу и способу нанесения лакокрасочные покрытия.
Классификация методик электрохимической катодной защиты
Такой способ предупреждения коррозии был предложен в 20-х годах XIX века и поначалу использовался в судостроении: медные корпуса кораблей обшивались протекторами-анодами, значительно снижающими скорость корродирования металла.
После того, как была установлена эффективность новой технологии, изобретение стало активно применяться в других областях промышленности. Через некоторое время оно было признано одним из самых эффективных способов защиты металлов.
В настоящее время используется два основных типа катодной защиты трубопроводов от коррозии:
- Самый простой способ: к металлическому изделию, требующему предохранения от коррозии, подводится внешний источник электрического тока. В таком исполнении сама деталь приобретает отрицательный заряд и становится катодом, роль же анода выполняют инертные, не зависящие от конструкции, электроды.
- Гальванический метод. Нуждающаяся в защите деталь соприкасается с защитной (протекторной) пластиной, изготавливаемой из металлов с большими значениями отрицательного электрического потенциала: алюминия, магния, цинка и их сплавов. Анодами в этом случае становятся оба металлических элемента, а медленное электрохимическое разрушение пластины-протектора гарантирует поддержание в стальном изделии требуемого катодного тока. Через более или менее долгое время, в зависимости от параметров пластины, она растворяется полностью.
Характеристики первого метода
Этот способ ЭХЗ трубопроводов, в силу простоты, наиболее распространён. Применятся он для предохранения крупных конструкций и элементов, в частности, трубопроводов подземного и наземного типов.
Методика помогает противостоять:
- питтинговой коррозии;
- коррозии из-за присутствия в зоне расположения элемента блуждающих токов;
- коррозии нержавеющей стали межкристального типа;
- растрескиванию латунных элементов вследствие повышенного напряжения.
Характеристики второго метода
Эта технология предназначается, в отличие от первой, в том числе для защиты изделий небольших размеров. Методика наиболее популярна в США, в то время как в Российской Федерации используется редко. Причина в том, что для проведения гальванической электрохимическая защита трубопроводов необходимо наличие на изделии изоляционного покрытия, а в России магистральные трубопроводы таким образом не обрабатываются.
Катодная защита
Реализация принципа катодной защиты может осуществляться одним из двух способов. Первый — подача отрицательного потенциала может происходить от специального источника электроэнергии, именуемого станцией катодной защиты.
При использовании катодных станций может возникнуть следующая проблема.
Электричество для установки требуемого потенциала нередко подается по длинному кабелю. Этот кабель подвержен действию молнии и некоторым другим электромагнитным влияниям. Для того, чтобы в результате не произошло перенапряжения, рекомендуется использовать комплексное решение ZANDZ.
Механизм взаимодействия
Процесс электрохимической коррозии зависит от химического состава материалов и особенностей внешней среды. Если так называемый технический металл покрыт влажной пленкой, то в каждом из указанных гальванических микроэлементов, которые образуются на поверхности, протекают две независимые реакции. Более активный компонент коррозионной пары отдает электроны (к примеру, цинк в паре Zn-Fe) и переходит в жидкую среду в качестве гидратированных ионов (то есть корродирует) по следующей реакции (анодный процесс):
М + nH2O = Mz+* nH2O + ze.
Эта часть поверхности является отрицательным полюсом локального микроэлемента, где металл электрохимически растворяется.
На менее активном участке поверхности, которая является положительным полюсом микроэлемента (железо в паре Zn-Fe), электроны связываются за счет протекания реакции восстановления (катодный процесс) по схеме:
Ox + ze = Red.
Таким образом, наличие окислителей в водяной пленке, которые способны связывать электроны, обеспечивает возможность дальнейшего хода анодного процесса. Соответственно, электрохимическая коррозия может развиваться только при условии одновременного протекания как анодного, так и катодного процессов. Вследствие торможения одного из них скорость окисления уменьшается.

Ржавеют… все!
Выше в статье упоминался такой известный центр борьбы с коррозией, как Шведский институт коррозии (ШИК) — одна из наиболее авторитетных организаций в данной области.
Раз в несколько лет ученые института проводят интересное исследование: берут кузова хорошо потрудившихся автомобилей, вырезают из них наиболее подверженные коррозии «фрагменты» (участки порогов, колесных арок, кромок дверей и т.д.) и оценивают степень их коррозионного поражения.
Важно отметить, что среди исследуемых кузовов есть как защищенные (оцинковкой и/или антикором), так и кузова без какой либо дополнительной антикоррозионной защиты (просто окрашенные детали). Так вот, ШИК утверждает, что наилучшей защитой автомобильного кузова является лишь сочетание «цинк плюс антикор»
А вот все остальные варианты, включая «просто оцинковку» или «просто антикор», по словам ученых — плохи
Так вот, ШИК утверждает, что наилучшей защитой автомобильного кузова является лишь сочетание «цинк плюс антикор». А вот все остальные варианты, включая «просто оцинковку» или «просто антикор», по словам ученых — плохи.
Причины и признаки электрохимической коррозии
Электрохимическая коррозия отличается от химической тем, что процесс разрушения проходит в системе электролитов, отчего внутри этой системы возникает электрический ток. Два сопряжённых процесса, анодный и катодный, приводят к удалению из кристаллической решетки металла неустойчивых атомов. Ионы при анодном переходят в раствор, а электроны от анодного процесса попадают в ловушку к веществу-окислителю и связываются деполяризатором.
Таким образом, деполяризация – это отвод с катодных участков свободных электронов, а деполяризатор – вещество, которое отвечает за этот процесс. Основные реакции происходят с участием водорода и кислорода в роли деполяризаторов.

Существует множество примеров электрохимической коррозии разного типа, которая оказывает воздействие на металлические поверхности в природе и проходит под влиянием различных условий. Водород при этом работает в кислой среде, а кислород – в нейтральной.
Практически все металлы подвергаются электрохимической коррозии, и по этому признаку их разбивают на 4 группы, определяют величину их электродного потенциала:
- активные коррозируют даже в той среде, где нет окислителей;
- среднеактивные вступают в реакцию окисления в кислотной среде;
- малоактивные не вступают в реакцию при отсутствии окислителей и в нейтральных, и в кислых средах;
- не вступают в реакцию – высокой стабильности (благородные металлы, палладий, золото, платина, иридий).

Но эта же реакция может протекать и в воде, в растворах оснований, солей и кислот. В узкоспециальном различии атмосферной коррозии различают почвенную и аэрационную, морскую и биологическую (протекающую под воздействием бактерий).
Есть даже электрическая коррозия, которая протекает под воздействием электрического тока, и является результатом работы блуждающих токов, возникающих там, где электрический ток используется человеком для осуществления определенной деятельности.
Гомогенная металлическая поверхность при этом разрушается из-за термодинамической неустойчивости к окружающей среде. А гетерогенная – из-за состава кристаллической решётки, в которой атомы одного металла держатся плотнее, чем атомы инородных вкраплений. Эти реакции отличаются скоростью протекания ионизации ионов, и восстановления окислительных компонентов окружающей среды.
Разрушение металлических поверхностей при электрохимической коррозии состоит в одновременном протекании двух процессов: анодного и катодного, и отличия процессов состоят в том, что растворение происходит на анодах, которые и контактируют с окружающей средой через множество микроэлектродов, которые входят в состав поверхности любого металла и замкнуты на себя.

Это интересно: Гибка и гнутье листового металла
Антикоррозионная защита — зачем она нужна
Коррозия представляет собой процесс, сопровождающийся разрушением поверхностных слоев конструкций из стали и чугуна, возникающий в результате электрохимического и химического воздействия. Негативным следствием этого становится серьезная порча металла, его разъедание, что не позволяет использовать его по назначению.
Экспертами было проведено достаточно доказательств тому, что ежегодно порядка 10% от общего объема добычи металла на планете уходит на устранение потерь, связанных с воздействием коррозии, из-за которой происходит расплавление металлов и полная потеря эксплуатационных свойств металлическими изделиями.
При первых признаках воздействия коррозии изделия из чугуна и стали становятся менее герметичными, прочными. В то же время ухудшаются такие качества, как теплопроводность, пластичность, отражательный потенциал и некоторые иные важные характеристики. В дальнейшем конструкции и вовсе нельзя применять по назначению.
Вдобавок к этому именно с коррозией связывают большинство производственных и бытовых аварий, а также и некоторые экологические катастрофы. Трубопроводы, используемые для транспортировки нефти и газа, имеющие значительные участки, покрытые ржавчиной, могут в любой момент лишиться своей герметичности, что может создать угрозу для здоровья людей и природы в результате прорыва подобных магистралей.
К сожалению, пока не удалось создать такой технологии, которая бы смогла полностью защитить стальные сплавы и металлы от коррозии. При этом имеются возможности для задержания и уменьшения негативных последствий подобных процессов. Эта задача решается посредством использования большого количества антикоррозионных средств и технологий.
Предлагаемые сегодня методы борьбы с коррозией могут быть представлены в виде следующих групп:
- Использование электрохимических методов защиты конструкций;
- Создание защитных покрытий;
- Разработка и производство новейших конструкционных материалов, демонстрирующих высокую стойкость к коррозионным процессам;
- Добавление в коррозионную среду особых соединений, благодаря которым можно замедлить распространение ржавчины;
- Грамотный подход к выбору подходящих деталей и конструкций из металлов для сферы строительства.
Основные способы защиты
Для борьбы с электрохимической коррозией, обусловленной образованием гальванической пары, применяются следующие основные меры:
- Использование металлов и сплавов, устойчивых к коррозии. Например, меди или алюминия, у которых на поверхности образуется тонкая оксидная пленка, защищающая от коррозии предметы, изготовленные из данных металлов. Или нержавеющей стали, в которую добавлены присадки, изменяющие внутреннюю структуру материала таким образом, чтобы в нем не было неоднородностей с разными электрохимическими потенциалами.
- Гальваническое покрытие. Например, на обычную сталь наносят слой меди. Именно такая защита применяется в готовых наборах заземлителей ZANDZ
- Покрытие из диэлектрического материала, устойчивое к влаге, например, краска или лак.
- Применение во влажных условиях, по возможности, однородных материалов.
- Катодная защита, суть которой заключается в приложении к защищаемому элементу отрицательного потенциала.
- Соединение оцинкованных заземлителей с арматурой в бетоне лишь через искровые разрядники, способные проводить частичные разряды молнии. Разница потенциалов между стальными и цинковыми элементами много меньше напряжения пробоя разрядника, поэтому в обычных условиях электрохимическая коррозия протекать не будет.
Металлическое защитное покрытие
Наиболее интересной и перспективной является электрохимическая защита от коррозии другим видом металла. По характеру защитного воздействия металлизированные покрытия подразделяют на анодные и катодные. Остановимся на этом моменте более подробно.
Анодным называется покрытие, образованное более активным (менее благородным) металлом, чем тот, что защищают. То есть осуществляется защита элементом, который стоит в ряду напряжений до основного материала (например, покрытие железа цинком или кадмием). При местных разрушениях защитного слоя корродировать будет менее благородный металл-покрытие. В зоне царапин и трещин образовывается локальный гальванический элемент, катодом в котором является ограждаемый металл, а анодом – покрытие, которое окисляется. Целостность такой защитной пленки значения не имеет. Однако чем она толще, тем медленнее будет развиваться электрохимическая коррозия, дольше будет длиться полезный эффект.
Катодным называется покрытие металлом с большим потенциалом, который в ряду напряжений стоит после защищаемого материала (например, напыление низколегированных сталей медью, оловом, никелем, серебром). Покрытие должно быть сплошным, так как при его повреждении образовываются локальные гальванические элементы, в которых основной металл будет анодом, а защитный слой – катодом.

Эффективные методы очистки меди
Провести чистку медных предметов несложно, для этого не понадобятся дорогостоящие средства. Вот самые популярные методики, применяемые в домашних условиях:
- Кетчуп. Взять немного томатного кетчупа, смазать им изделие, оставить на две минуты. После ополоснуть струей воды.
- Раствор для мытья посуды. Намылить хозяйственную губку обычным средством для посуды, тщательно протереть поверхность, смыть водой. Этот способ лучше всего подходит для изделий, которые лишь немного потускнели.
- Лимон. Натереть медную поверхность долькой лимона, после пройтись по ней щеткой с жесткими ворсинками и помыть водой.
- Уксус и мука. Влить в чашку немного уксуса, добавить муку до получения теста средней густоты. Смазать медь тестом, оставить до высыхания, потом удалить остатки, а изделие натереть мягкой тряпочкой.
- Уксус и соль. Налить в кастрюлю из нержавеющей стали уксус 9%, всыпать немного соли, дать закипеть. Огонь выключить, в раствор положить медный предмет, не убирать его до остывания жидкости. Этот способ подходит для сильно загрязненных поверхностей.
Разновидность металлов по отношению к коррозии электрохимического вида
Все металлы по отношению к такому виду ржавчины делятся на 4 подтипа:
- Активные вещества или материалы с высокими параметрами термодинамической нестабильности. Это все щелочные виды металлов. Они подвержены влиянию коррозии даже в абсолютно нейтральных средах, где нет кислорода и других окислительных веществ.
- Средние материалы по уровню активности — в таблице Менделеева расположены между кадмием и водородом. Это материалы отличающиеся термодинамической нестабильностью в агрессивных кислых средах.
- Материалы с низкими параметрами активности или вещества с промежуточными параметрами стабильности по термодинамике. Противостоят коррозии в кислых и нейтральных атмосферах, при отсутствии кислорода.
- Благородные разновидности веществ. Это материалы с высокой стабильностью. Они поддаются коррозии только в кислых средах и в присутствии сильнейших окислителей.
Такие типы ржавчины могут разделяться по видам агрессивных сред, в которой она протекает:
- Процесс в электролитных веществах — процесс протекает в жидких кислых, щелочных средах, а также в простой воде.
- Атмосферный вид — любой газовый вариант с наличием влажности. Это очень распространенный вариант электрохимического разрушения металла. Главное, чтобы в данной среде была влажность. Только при таких условиях есть возможность протекания необходимых реакций.
При электрохимической вариации процесса одна часть металла служит анодом, а другая — катодом. Последним становятся те участки металла, куда больше поступает кислорода.
В зависимости от воздействующих сред есть и другие разновидности коррозий:
- Почвенная — протекает с разной степенью интенсивности. Все зависит от агрессивности почвы. В таких условиях происходит подземные разрушительные процессы на трубах и прочих подземных конструкциях.
- Аэрационная — причиной служит неравномерный приток воздуха к разным участкам материала.
- Морская — процесс проходит строго в соленой воде.
- Биокоррозия — результат жизнедеятельности бактерий и микроорганизмов. Они выделяют газы, которые и приводят к возникновению разрушительных процессов.
- Электрокоррозия — является результатом воздействия блуждающего тока.
Кроме того основные виды коррозии могут различаться в зависимости от типа металла, на которых они возникают.
Химическая коррозия
Как известно, даже в сухом воздухе при обычной температуре металлы и сплавы изменяются. Блестящая глянцевитая поверхность металла тускнеет, становится матовой. Это объясняется тем, что металл покрывается тончайшей плёнкой окисла — продуктов взаимодействия металла и кислорода воздуха. Повышение температуры ускоряет этот процесс. Если образующаяся на поверхности металла окисная плёнка плотная, как, например, у алюминия или цинка, то она предохраняет металл от дальнейшего окисления и играет своего рода защитную роль для него. На других металлах, в частности на железе, поверхностная плёнка имеет поры, через которые проникает кислород воздуха, вследствие чего такая плёнка не препятствует дальнейшему разрушению металла.
Образование плёнок на поверхности металлов связано с влиянием не только кислорода, но и других газов, находящихся в воздухе. С металлом реагирует сернистый газ, углекислый газ и др. Эти газы при совместном воздействии водяных паров воздуха очень быстро разрушают металл.
Некоторые минеральные кислоты, как, например, серная и азотная, так же как и кислород воздуха, при взаимодействии с металлом образуют на его поверхности плотную окисную плёнку. Так, например, если пластинку железа с хорошо очищенной поверхностью поместить в концентрированную азотную кислоту, то на поверхности возникает прочная окисная плёнка, предохраняющая железо от его дальнейшего растворения. В этом случае говорят, что азотная кислота пассивирует железо. Однако если такую же пластинку, предварительно не обработанную концентрированной азотной кислотой, опустить в ту же кислоту, но разбавленную, она быстро будет разрушаться. Точно так же концентрированная серная кислота пассивирует поверхность железа, предохраняя его от дальнейшего разрушения.
Химическая коррозия особенно быстро протекает в присутствии влаги, углекислого газа и кислорода воздуха. На поверхности железных изделий в этих случаях образуется слой ржавчины. Оксид железа покрывает его хрупким и пористым слоем. Поэтому такой окисный слой не предохраняет металл от дальнейшего ржавления. Химическая коррозия, особенно газовая, приносит громадный ущерб народному хозяйству. Не меньший вред почти всем отраслям народного хозяйства причиняет и электрохимичесиая коррозия.


































